Un modelo atómico es una representación grafica de la materia a nivel atómico. Tiene como finalidad la facilitación de su estudio atreves de la abstracción de la lógica de un átomo en una esquema.
Estructura del átomo
En el átomo distinguimos dos partes: el núcleo y la corteza.
- El núcleo es la parte central del átomo y contiene partículas con carga positiva, los protones, y partículas que no poseen carga eléctrica, es decir son neutras, los neutrones. La masa de un protón es aproximadamente igual a la de un neutrón.
- Todos los átomos de un elemento químico tienen en el núcleo el mismo número de protones. Este número, que caracteriza a cada elemento y lo distingue de los demás, es el número atómico y se representa con la letra Z.
- La corteza es la parte exterior del átomo. En ella se encuentran los electrones, con carga negativa. Éstos, ordenados en distintos niveles, giran alrededor del núcleo. La masa de un electrón es unas 2000 veces menor que la de un protón.
- Los átomos son eléctricamente neutros, debido a que tienen igual número de protones que de electrones. Así, el número atómico también coincide con el número de electrones.
| Año | Científico | Descubrimientos experimentales | Modelo atómico | ||||||
| 1808 |  John Dalton |
| 
| ||||||
| 1897 |  J.J. Thomson |
| 
| ||||||
| 1911 |  E. Rutherford | 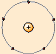
| |||||||





No hay comentarios:
Publicar un comentario